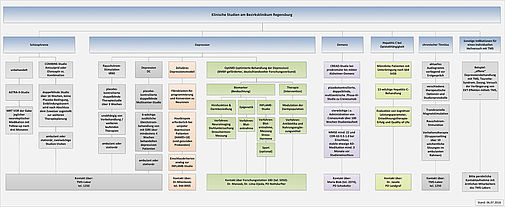
Allgemeine Information zu klinischen Studien
Hier finden Sie wichtige Informationen zur Bedeutung und Durchführung klinischer Studien
Was sind klinische Studien?
Klinische Studien dienen der Weiter- und Neuentwicklung von Arzneimitteln zur Verbesserung der Behandlungsmöglichkeiten erkrankter Patienten. Klinische Prüfungen finden in so genannten Prüfzentren statt wie zum Beispiel Forschungseinrichtungen, Kliniken, aber auch Arztpraxen. Dabei arbeiten die pharmazeutischen Unternehmen mit den zuständigen Behörden und durchführenden Medizinern zusammen.
-->Warum sind klinische Studien nötig?
Gegen etwa ein Drittel der bekannten Krankheiten gibt es noch keine adäquate medikamentöse Behandlungsmöglichkeit. Aber nicht nur gegen diese Erkrankungen müssen Arzneimittel entwickelt werden, vorhandene Arzneimittel müssen auch weiterentwickelt werden bzw. neue, verträglichere Medikamente gefunden werden.
Bevor ein Medikament auf den Markt kommt, muss es einen langen Weg der Prüfung bestehen. Die rechtliche Grundlage für den Ablauf klinischer Studien bildet das Arzneimittelgesetz (AMG). Bevor es am Menschen getestet wird, wird es in Zellkulturen und isolierten Tierorganen geprüft.
Die Suche nach neuen Wirkstoffen ist jedoch mühsam, von 10000 erforschten Substanzen erreicht nur ein einziges die Zulassung. Somit kostet die Entwicklung eines neuen Medikamentes ca. 500 Mill. Euro, die Zeitdauer von der "Entdeckung" der Substanz bis zur Zulassung beträgt ca. 15 Jahre.
Welche Unterschiede gibt es zwischen einzelnen Studien?
Die Prüfung am Menschen durchläuft verschiedene Phasen (I-III), aber auch nach Zulassung eines neuen Medikamentes wird weitergeforscht (Phase IV).
Etwa fünf Jahre nach den ersten Laboruntersuchungen werden zunächst Tests an freiwilligen, gesunden Probanden gestartet (Phase I-Studie). Hier wird unter anderem die Verträglichkeit getestet, die Zahl der Teilnehmer ist vergleichsweise gering (ca. 50 gesunde Teilnehmer).
In den Phase-II-Studien nehmen erkrankte Probanden teil (ca. 500), in diesen Studien wird unter anderem die Wirksamkeit untersucht, ebenso wie bei den vor der Zulassung stattfindenden Phase-III-Studien (grosse Anzahl von Teilnehmern), welche neben der Wirksamkeit unter anderem auch ökonomische Aspekte und Lebensqualität berücksichtigen. Die Phase-IV-Studien finden nach Zulassung statt, hier werden weiterhin Daten zu Wirkung und Nebenwirkungen erfasst.
Sind Pharmastudien für Teilnehmer gefährlich?
In Phase-I-Studien, in denen die unter anderem die Verträglichkeit von neuen Substanzen getestet wird, besteht das Risiko von unerwünschten Arzneimittelwirkungen, die sich in den vorhergehenden Tierversuchen noch nicht vorhersehen liessen und/oder potentiell gefährlich sein können. Daher werden diese Studien an gesunden Probanden getestet, die über dieses Risiko ausführlich aufgeklärt werden und dementsprechend hoch vergütet werden.
Ab Phase-II-Studien ist das Risiko für schwere, unerwünschte und/oder unbekannten Arzneimittelwirkungen vergleichsweise gering. Es wird unter anderem die Wirksamkeit von neuen Substanzen getestet, eine Vergütung für die Teilnahme ist deshalb in Deutschland untersagt, allerdings kann eine Aufwandsentschädigung bezahlt werden. Die Teilnehmer bei diesen Studien gehen meist in die Hunderte.
Bei Phase-IV-Studien wird ein schon zugelassenes Arzneimittel getestet, die Gefahr von Nebenwirkungen ist also gleichzusetzen mit dem Nebenwirkungsrisiko von Nichtstudienpatienten in der regulären ärztlichen Versorgung.
Welchen Nutzen habe ich durch die Teilnahme?
Welchen Nutzen habe ich durch die Teilnahme an einer klinischen Studie?
Ihnen und Ihrer Krankenkasse entstehen keine Kosten. Die Kosten für die ärztliche Betreuung und die Medikamente übernimmt der Auftraggeber. Neben einer ausführlichen Aufklärung besteht für den Teilnehmer ein besonderer Versicherungsschutz, die nötigen Untersuchungen (Blutwerte, EKG, körperliche Untersuchung, etc.) gehen oft über das bei regulärer ambulanter Behandlung erforderliche Maß hinaus.
-->Wie kann ich mich eingehender informieren?
Das Koordinierungsnetzwerk für klinische Studien stellt auf seiner Webseite detaillierte Informationen bereit unter www.kks-netzwerk.de.
-->Welche Voraussetzungen müssen erfüllt sein?
Welche Voraussetzungen müssen erfüllt sein, um an einer klinischen Prüfung teilnehmen zu können?
Um als Erkrankter teilnehmen zu können, müssen neben der geeigneten Diagnose vielfältige Kriterien erfüllt sein, die allerdings sehr studienspezifisch sind.
Man muss in jedem Fall volljährig sein.
Patienteninformationen zu klinischen Studien
"Auf Hirn und Darm geprüft.... Depression besser verstehen"
"Therapiestudie Minocyclin bei Depression"
Lehrstuhl für Psychiatrie und Psychotherapie
Universitätsstraße 84
93053 Regensburg
Telefon 0941 941-1004
E-Mail
rainer.rupprecht@medbo.de